2021-12-17 13:33 | 來源:中國(guó)網(wǎng)財(cái)經(jīng) | 作者:俠名 | [科創(chuàng)板] 字號(hào)變大| 字號(hào)變小
新通藥物計(jì)劃采用科創(chuàng)板第五套上市標(biāo)準(zhǔn)申請(qǐng)上市,但公司上市前的增資估值低于該標(biāo)準(zhǔn)規(guī)定的“預(yù)計(jì)市值不低于人民幣40億元”的要求。......

西安新通藥物研究股份有限公司(“新通藥物”)向上交所科創(chuàng)板發(fā)起沖擊,上市申請(qǐng)于12月6日獲受理。
記者梳理發(fā)現(xiàn),新通藥物成立21年來,因無核心產(chǎn)品實(shí)現(xiàn)商業(yè)化生產(chǎn)和銷售,目前仍處于虧損階段,近三年凈虧已達(dá)2.63億。
另外,新通藥物計(jì)劃采用科創(chuàng)板第五套上市標(biāo)準(zhǔn)申請(qǐng)上市,但公司上市前的增資估值低于該標(biāo)準(zhǔn)規(guī)定的“預(yù)計(jì)市值不低于人民幣40億元”的要求。
對(duì)此,中國(guó)網(wǎng)財(cái)經(jīng)致函新通藥物,截止發(fā)稿,未收到任何回復(fù)。
三年凈虧2.63億無核心產(chǎn)品商業(yè)化
有媒體報(bào)道稱,根據(jù)招股書披露,在2020年10月的增資中,北京阜瑞、高明、山東科創(chuàng)、西高投、峨勝集團(tuán)對(duì)新通有限進(jìn)行增資,價(jià)格為64.76元/注冊(cè)資本,由此測(cè)算新通有限當(dāng)時(shí)的投后估值約為30億元,低于科創(chuàng)板第五套上市標(biāo)準(zhǔn)要求的40億元。此外,2020年12月新通有限兩位股東漢富璟晟與潤(rùn)耀輝華進(jìn)行了股權(quán)轉(zhuǎn)讓,當(dāng)時(shí)的估值為不到25億元,也明顯低于40億元。
資料顯示,新通藥物成立于2000年5月30日,是一家專注藥物研發(fā)的高新技術(shù)企業(yè),現(xiàn)聚焦于慢性乙肝、肝癌、癲癇等重大疾病領(lǐng)域。
此次IPO擬募集資金12.79億元,其中近七成用于新藥研發(fā)項(xiàng)目,其余3成用于創(chuàng)新藥物產(chǎn)業(yè)化生產(chǎn)基地建設(shè)項(xiàng)目以及補(bǔ)充流動(dòng)資金。
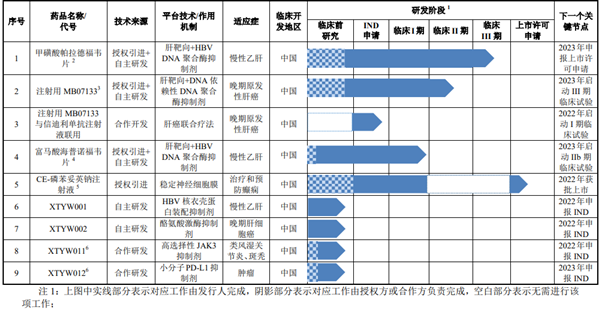
不過,記者注意到,公司9款在研項(xiàng)目中,只有CE-磷苯妥英鈉注射液、富馬酸海普諾福韋片、注射用MB07133和甲磺酸帕拉德福韋片分別處于上市許可申請(qǐng)、臨床I期、臨床II期和臨床III期臨床階段,而其余5款產(chǎn)品還未進(jìn)入臨床。目前公司并無核心產(chǎn)品實(shí)現(xiàn)商業(yè)化生產(chǎn)和銷售。
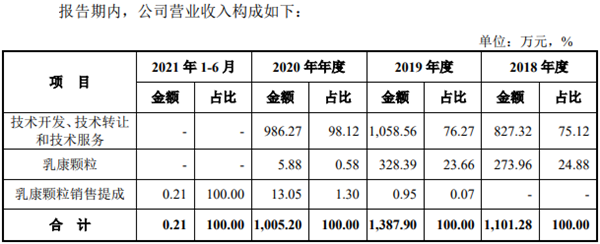
數(shù)據(jù)顯示,2018年-2021年上半年,公司分別實(shí)現(xiàn)營(yíng)收1101.28萬元、1387.90萬元、1005.20萬元及0.21萬元,主要依靠技術(shù)服務(wù)、技術(shù)轉(zhuǎn)讓和技術(shù)開發(fā)相關(guān)項(xiàng)目的服務(wù)收入及乳康顆粒的銷售收入。其中依靠銷售乳康顆粒獲得的收入分別為1101.28萬元、1387.90萬元、1005.20萬元和0.21萬元。
值得注意的是,2019年新通藥物向千禾藥業(yè)轉(zhuǎn)讓乳康顆粒專利及新藥證書,2020年除了銷售庫(kù)存商品之后不再進(jìn)行乳康顆粒的生產(chǎn),這也導(dǎo)致2021年上半年新通藥物收入僅2085.52元。
缺少造血的新通藥物只能依靠政府補(bǔ)助、稅反和對(duì)外融資等途徑獲得資金。報(bào)告期內(nèi),新通藥物政府補(bǔ)助金額分別為1440.28萬元、916.54萬元、414.28萬元和413.88萬元。
然而,盡管政府補(bǔ)助可為公司緩解些許壓力,但也只是稍解“燃眉之急”,營(yíng)運(yùn)資金仍然承壓。
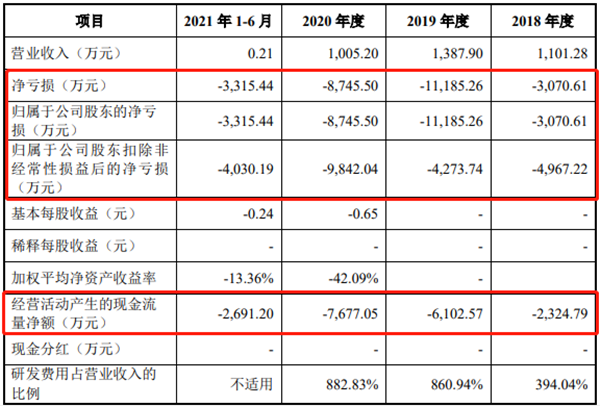
報(bào)告期公司經(jīng)營(yíng)現(xiàn)金流凈額分別為-2324.79萬元、-6102.57萬元、-7677.05萬元和-2691.28萬元。2019年由于新通藥物收到的政府補(bǔ)助減少1326.03萬元,收到的稅收返還減少203.93萬元,該年公司現(xiàn)金流凈額同比下降了162.50%;2020年公司注射用MB07133研發(fā)項(xiàng)目進(jìn)入臨床II期試驗(yàn);甲磺酸帕拉德福韋得研發(fā)進(jìn)入III期臨床試驗(yàn)又進(jìn)一步增加了臨床費(fèi)用支出,新通藥物該年現(xiàn)金流量?jī)纛~較2019年下降25.80%。
招股書顯示,報(bào)告期新通藥物的歸母凈利潤(rùn)分別為-3070.61萬元、-1.11億元、-8745.50萬元和-3315.44萬元,扣非后歸母凈利潤(rùn)分別為-4967.22萬元、-4273.74萬元、-9842.04萬元和-4030.19萬元。截至2021年上半年,新通藥物累計(jì)未彌補(bǔ)虧損達(dá)1.05億元。
然而在業(yè)績(jī)持續(xù)虧損并預(yù)計(jì)未來將繼續(xù)虧損的情況下,新通藥物仍投入大量資金用于產(chǎn)品管線的臨床前研究、臨床試驗(yàn)及新藥上市前準(zhǔn)備。2018年、2019年、2020年及2021年1-6月,公司研發(fā)費(fèi)用分別為4,339.49萬元、11,948.97萬元、8,874.23萬元和3,033.96萬元,累計(jì)達(dá)2.82億元。
對(duì)此,新通藥物表示,新藥研發(fā)需要大量持續(xù)的研發(fā)投入以及由于股權(quán)激勵(lì)產(chǎn)生的股份支付費(fèi)用。隨著公司更多在研藥品進(jìn)入臨床試驗(yàn)階段、現(xiàn)有臨床試驗(yàn)的繼續(xù)推進(jìn)以及未來產(chǎn)品的商業(yè)化推廣,未來幾年將存在持續(xù)大規(guī)模的研發(fā)投入。
部分專利為授權(quán)獲得“licencein”模式不等于創(chuàng)新
不過,高額的研發(fā)費(fèi)用支出并不意味著高額回報(bào),一款新藥的變現(xiàn)過程漫長(zhǎng)而充滿不確定性。曾有統(tǒng)計(jì)稱,一個(gè)原創(chuàng)新藥最后成為商品正式投入市場(chǎng)的成本超過10億美元,大約花費(fèi)約10年時(shí)間,藥物篩選的失敗率高達(dá)97%。
據(jù)了解,目前新通制藥進(jìn)展最快的在研產(chǎn)品——CE-磷苯妥英鈉注射液是一款依托磺丁基-β-環(huán)糊精鈉(商品名:Captisol?)包合技術(shù)的改良型磷苯妥英鈉注射液,用于治療全身強(qiáng)直一陣孿性癲癇持續(xù)狀態(tài),預(yù)防和治療神經(jīng)外科圍手術(shù)中引起的癲癇發(fā)作。
新通藥物表示,該產(chǎn)品有望成為中國(guó)首個(gè)獲批預(yù)防和治療神經(jīng)外科圍手術(shù)期和手術(shù)中引起的癲癇發(fā)作適應(yīng)癥藥品。
記者注意到,這款產(chǎn)品的技術(shù)來源于合作方授權(quán),是新通藥物向Sedor公司引進(jìn)的產(chǎn)品,為磷苯妥英鈉注射液的改良型藥物,作為2.2類新藥申請(qǐng)IND。由于Sedor公司的同類產(chǎn)品已于2020年11月由FDA批準(zhǔn)在美國(guó)上市,據(jù)相關(guān)法規(guī),在申報(bào)許可上市時(shí)按化學(xué)藥三類申報(bào)。
根據(jù)新通藥物與美國(guó)Sedor公司2017年6月簽署的《許可與分許可協(xié)議》顯示,Sedor公司擁有CyDex公司Captisol?藥物配制系統(tǒng)用于CE-磷苯妥英鈉注射液的全球獨(dú)占許可,Sedor公司授予發(fā)行人對(duì)于Captisol?藥物配制系統(tǒng)(分許可知識(shí)產(chǎn)權(quán)及Captisol數(shù)據(jù)包)在中國(guó)(含香港特別行政區(qū),不含中國(guó)臺(tái)灣)用于CE磷苯妥英鈉注射液的獨(dú)占許可。
同樣的,公司另一款核心在研產(chǎn)品甲磺酸帕拉德福韋片項(xiàng)目在新通藥物引進(jìn)前已由Metabasis公司在美國(guó)完成了II期臨床試驗(yàn),后由凱華公司(新通藥物于2015年收購(gòu)的全資子公司)于2011年1月引進(jìn)。產(chǎn)品授權(quán)引進(jìn)后公司開展臨床前藥學(xué)研究,補(bǔ)充了臨床前安全性研究,并按照原CFDA的法規(guī)要求在中國(guó)對(duì)其進(jìn)行了臨床試驗(yàn),已完成I期、II期臨床試驗(yàn),目前正處于III期臨床試驗(yàn)階段。
除此之外,注射用MB07133在公司引進(jìn)前也由Metabasis公司在美國(guó)完成了I期臨床試驗(yàn)、富馬酸海普諾福韋片在引進(jìn)前,其化合物專利同樣系Metabasis公司擁有。
另治療類風(fēng)濕關(guān)節(jié)炎、斑禿的XTYW011和腫瘤適應(yīng)癥XTYW2兩款處于臨床前研究的藥物系新通藥物與中國(guó)藥科大學(xué)的合作研發(fā)項(xiàng)目。雙方約定共同完成臨床前研究,后續(xù)工作將由新通藥物完成。
截至招股書發(fā)行前,新通藥物已取得17項(xiàng)發(fā)明專利,7項(xiàng)授權(quán)許可專利,其中三項(xiàng)來自Metabasis公司、四項(xiàng)來自CyDex公司,涉及核心產(chǎn)品。
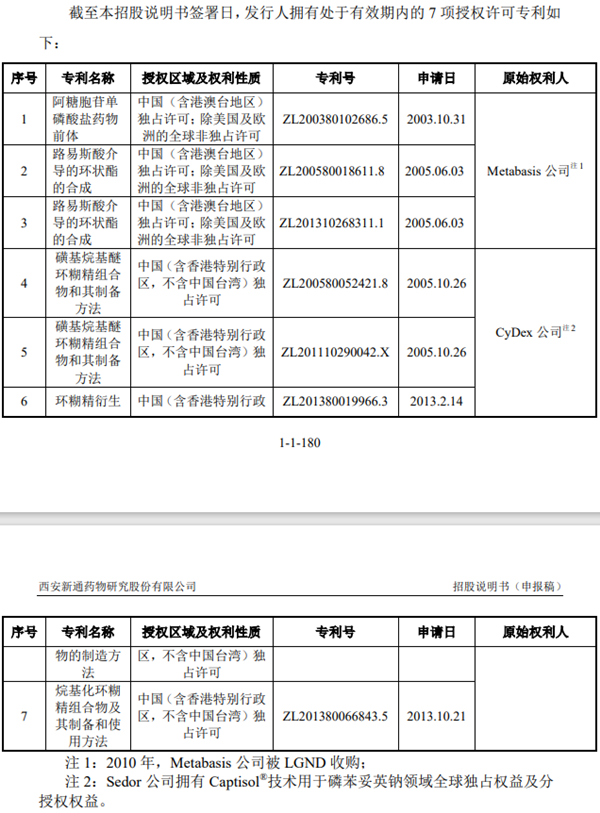
從研發(fā)管線來看,新通藥物是一家典型的“licencein”公司,即授權(quán)引進(jìn),“產(chǎn)品引進(jìn)方”向“產(chǎn)品授權(quán)方”支付一定的首付款,并約定一定金額的里程碑費(fèi)用(按品種開發(fā)進(jìn)展)以及未來的銷售提成,從而獲得產(chǎn)品在某些國(guó)家(地區(qū))的研發(fā)、生產(chǎn)及銷售的商業(yè)化權(quán)利。
“licencein”無疑是快速學(xué)習(xí)國(guó)外成果的窗口,曾風(fēng)靡整個(gè)醫(yī)藥市場(chǎng)。不過近年,資本市場(chǎng)有聲音“科創(chuàng)板開始對(duì)Licensein模式的生物醫(yī)藥企業(yè)從嚴(yán)審查。”
據(jù)此前科創(chuàng)板發(fā)審經(jīng)驗(yàn)顯示,如果生物醫(yī)藥企業(yè)有大量的licensein管線,那么“科創(chuàng)屬性”將在企業(yè)上市問詢中被重點(diǎn)關(guān)注。在CDE強(qiáng)調(diào)“臨床價(jià)值”后,甚至曾有一批以licensein為主要模式的生物醫(yī)藥企業(yè)被攔在了科創(chuàng)板的大門之外。
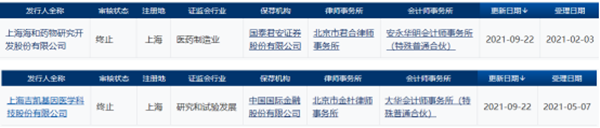
記者注意到,今年9月,上市委連續(xù)否決了兩家生物醫(yī)藥企業(yè),分別是海和藥物、吉?jiǎng)P基因。其中,海和藥物被質(zhì)問“引進(jìn)或合作開發(fā)的核心產(chǎn)品是否獨(dú)立自主進(jìn)行過實(shí)質(zhì)性改進(jìn)、對(duì)合作方是否構(gòu)成技術(shù)依賴”;吉?jiǎng)P基因則被問“核心技術(shù)是否具有先進(jìn)性”。
同類藥物已進(jìn)“4+7城市藥品集采”內(nèi)卷再度加劇
作為一家專注于慢性乙肝、肝癌、癲癇等重大疾病領(lǐng)域治療的創(chuàng)新藥企業(yè),新通藥物一方面面臨著專利到期的“內(nèi)憂”,一方面面臨同類藥品、技術(shù)升級(jí)、產(chǎn)品迭代的“外患”。
招股書顯示,新通藥物核心在研產(chǎn)品甲磺酸帕拉德福韋片、富馬酸海普諾福韋片的化合物結(jié)構(gòu)的中國(guó)專利已于2020年3月3日到期,而其研發(fā)進(jìn)展仍分別處于臨床Ⅲ期、臨床Ⅰ期;注射用MB07133的化合物結(jié)構(gòu)的中國(guó)專利將于2023年10月31日到期,研發(fā)進(jìn)展處于臨床Ⅱ期;CE-磷苯妥英鈉注射液藥品組合物專利將于2036年到期,目前處于上市許可申請(qǐng)。
根據(jù)《中華人民共和國(guó)藥品管理法實(shí)施條例》對(duì)批準(zhǔn)生產(chǎn)的新藥設(shè)置了最長(zhǎng)5年的新藥監(jiān)測(cè)期規(guī)定,在這一期間,該制度將有效的阻止仿制藥的上市。
值得注意的是,由于Sedor公司的同類產(chǎn)品已于2020年11月由FDA批準(zhǔn)在美國(guó)上市,據(jù)相關(guān)法規(guī),CE-磷苯妥英鈉注射液在申報(bào)許可上市時(shí)按化學(xué)藥三類申報(bào)。而化學(xué)藥三類藥物不適用于“新藥監(jiān)測(cè)期”制度。
“專利到期”意味著“相關(guān)仿制藥誕生”,將進(jìn)一步加劇市場(chǎng)競(jìng)爭(zhēng),或?qū)е鹿菊{(diào)低現(xiàn)有產(chǎn)品價(jià)格。
另一方面,“外患”亦在不斷給公司施壓。招股書顯示,公司的核心產(chǎn)品甲磺酸帕拉德福韋片、富馬酸海普諾福韋片屬于依托肝靶向創(chuàng)新藥物研發(fā)平臺(tái)研發(fā)的治療慢性乙肝的1類創(chuàng)新藥。
記者注意到,目前已有恩替卡韋片(ETV)、富馬酸替諾福韋二吡呋酯片(TDF)、富馬酸丙酚替諾福韋片(TAF)、艾米替諾福韋片(TMF)等多款同類藥物在國(guó)內(nèi)獲批上市銷售,并有多個(gè)同類藥物處于不同的臨床試驗(yàn)階段。
并且ETV、TDF已被納入4+7城市藥品集中采購(gòu)目錄及聯(lián)盟地區(qū)藥品集中采購(gòu)目錄,相關(guān)藥物銷售價(jià)格大幅下降。而在乙肝治療領(lǐng)域,ETV、TDF與甲磺酸帕拉德福韋片、富馬酸海普諾福韋片存在競(jìng)爭(zhēng)關(guān)系。
同樣的,公司另一款產(chǎn)品注射用MB07133屬于依托肝靶向創(chuàng)新藥物研發(fā)平臺(tái)研發(fā)的二線治療晚期肝細(xì)胞癌的1類創(chuàng)新藥。
目前,已有瑞戈非尼、PD-1單抗(替雷利珠單抗注射液和注射用卡瑞利珠單抗等)、阿帕替尼等多款同類藥物在國(guó)內(nèi)獲批上市銷售,并有多個(gè)同類藥物處于不同的臨床試驗(yàn)階段。
對(duì)此,新通制藥在招股書中坦言,若公司在研藥品相關(guān)領(lǐng)域出現(xiàn)突破性進(jìn)展,或公司藥物治療領(lǐng)域內(nèi)誕生更具競(jìng)爭(zhēng)優(yōu)勢(shì)的創(chuàng)新藥物,公司在研產(chǎn)品可能面臨被市場(chǎng)淘汰、失去商業(yè)價(jià)值的風(fēng)險(xiǎn),從而對(duì)公司的持續(xù)盈利能力產(chǎn)生重大不利影響。
1.本站遵循行業(yè)規(guī)范,任何轉(zhuǎn)載的稿件都會(huì)明確標(biāo)注作者和來源;2.本站的原創(chuàng)文章,請(qǐng)轉(zhuǎn)載時(shí)務(wù)必注明文章作者和來源,不尊重原創(chuàng)的行為我們將追究責(zé)任;3.作者投稿可能會(huì)經(jīng)我們編輯修改或補(bǔ)充。
熱門






4
5
6
7
8
9
10

信息產(chǎn)業(yè)部備案/許可證編號(hào): 京ICP備17002173號(hào)-2 電鰻快報(bào)2013-2023 www.shhai01.com
相關(guān)新聞